لقاح الفيروس الحليمي البشري 18، 16 والوقاية من سرطان عنق الرحم في الدول النامية:
المستتبعات السياسية
ملخص:
تحدث 70% تقريباً من حالات الإصابة بسرطان عنق الرحم على مستوى العالم بسبب الأنماط الوراثية ١٦ و ١٨ لفيروس الورم الحليمي البشري (HPV) وهو فيروس ينتقل بالإتصال الجنسي. ومع توفر لقاح فعال ضد هذين النمطين من فيروس الورم الحُليمي البشري تظهر بارقة أمل حقيقية في الحد من العبء العالمي لسرطان عنق الرحم في الدول النامية. يجب على الأطراف المعنية التي تواجهها قرارات بشأن أين تستثمر الأموال في مجال تحسين الصحة أن تضع في الاعتبار عبء المرض المتسبب فيه سرطان عنق الرحم مقارنة بالأولويات الأخرى، فضلاً عن المزايا المقارنة للتدخلات المختلفة. لقد أجرينا سلسلة من التحليلات الحصول على معلومات حول مزايا والتكلفة المطلوبة ومردود التكلفة الخاصة بلقاح فيروس الورم الحُليمي البشري (16، 18). لكي تكون هذه المعلومات متاحة للوكالات التي تعد التوصيات الخاصة بسياسة التطعيمات وآليات تنسيق التمويل، وكذلك لصُناع القرار على مستوى البلدان. وقد وجد أن توفير لقاح فيروس الورم الحُليمي البشري لنسبة ٧٠% من الفتيات في عمر المراهقة في ٧٢ من البلدان الأكثر فقرًا في العالم، مثل الصين وتايلاند ودول أمريكا اللاتينية ومنطقة الكاريبي، من شأنه أن يحول في المستقبل دون وفاة ما يزيد على أربعة ملايين امرأة ممن سيأخذن اللقاح خلال العقد القادم.
ويمكن أن تكون مردود التكلفة جيدة حتى في البلدان الفقيرة؛ شريطة أن لا تزيد تكلفة لقاح فيروس الورم الحُليمي البشري على ١٠ – ٢٥ دولاراً لكل مراهقة. إن بواعث القلق بشأن التكاليف المالية ومدى القدرة على شراء اللقاح تبرز الحاجة إلى خفض أسعار اللقاح وتوفير آليات تتصف بمردود التكلفة، فيما يخص إتاحة اللقاح للفتيات في سن المراهقة، وللموصول إلى مصادر تمويل مبتكرة.
Benefits, cost requirements and cost-effectiveness of the HPV16,18 vaccine for cervical cancer Prevention in developing countries: policy implications Sue J Goldie, Meredith O’Shea, Mireia Diaz, Sun-Young Kim Reproductive Health Matters 2008;16(32):86-96
تمثل الوفيات الممكن تجنبها ما بين النساء في الدول النامية بسبب سرطان عنق الرحم أحد أوجه القصور الأكثر مأساوية على الإطلاق في مجال الصحة العامة. تصل نسبة النساء ممن يتعرضن للإصابة بسرطان عنق الرحم إلى نصف مليون امرأة سنويًا؛ وتوجد أعلى النسب ما بين البلدان النامية حيث لم تكن برامج المسوح مجدية. تحدث حوالي ٨٠% من حالات الوفيات الحالية بسبب سرطان عنق الرحم في البلدان النامية؛ ومن المتوقع أن تصل هذه النسبة إلى ٩٠% بحلول عام ٢٠٢٠(1)
فيروس الورم الحُليمي البشري من أكثر الفيروسات التي تنتقل عبر الاتصال الجنسي شيوعًا, وهو السبب المعروف المسئول عن سرطان عنق الرحم. على الرغم من التفاوت الوبائي الملحوظ فإن نمطى فيروس الورم الحُليمي البشرى (۱٦ ، ۱۸) يتسببان في حوالي 70% من حالات سرطان عنق الرحم؛ (2 – 4) بينما تتسبب الأنماط الجينية الثمانية الأكثر شيوعًا لفيروس الورم الحُليمي البشري (١٦ , ١٨، ٤٥ , ٣١ ، ٣٣ ، 52, 58, 35) في نسبة ٩٠% من حالات سرطان الشرج و ٤٠% من السرطانات المتعلقة بالمنطقة الشرجية التناسلية وعلى الأقل 12% من حالات سرطانات الفم والبلعوم. (۱) تأتي التباينات الإقليمية في معدلات الإصابة بسرطان عنق الرحم نتيجة الإختلافات الكامنة في إنتشار أنماط فيروس الورم الحُليمي البشري عالية الخطورة وكذا للتفاوتات في مدى توفر الوقاية الفعالة من سرطان عنق الرحم والعلاج منه.
بخلاف معظم أنواع السرطان، من الممكن الوقاية من على سرطان عنق الرحم من خلال الفحص الدوري لإكتشاف وإزالة الأنسجة المصابة بتغيرات خلوية في مرحلة ما قبل التسرطن. من الممكن لبرنامج المسح التقليدي أن يتطلب نحو ثلاث زيارات لجمع عينات من خلايا عنق الرحم وإجراء تقييم تشخيصي ثم تقديم العلاج اللازم. في البلدان التي استطاعت الوصول إلى تغطية مرتفعة للشابات المستخدمات للفحص الخلوي على فترات متواترة، انخفضت نسبة الوفيات فيها بشكل ملحوظ. بيد أنه في البلدان ذات الموارد المحدودة والبنية التحتية الصحية غير الملائمة ثبت صعوبة تنفيذ الفحص المنظم.(5)
تأتي الفرص الجديدة للحد من وفيات سرطان عنق الرحم من خلال بدائل جديدة وأكثر جدوى المسوح من أجل البلدان النامية، ومؤخرًا أيضًا باستخدام اللقاحات الوقائية ضد أنماط فيروس الورم الحُليمي البشري المتسببة في السرطان. تتضمن مناهج المسوح الواعدة، التي أثبتت فاعليتها ومردوية تكاليفها، اختبار الحمض النووي للفيروس الحُليمي البشري، ومقاربة الفحص البصري، مع سبب تركيز الإهتمام على فحص النساء ما بين ٣٠ – ٤٥ عاماً من مرة إلى ثلاث مرات في العمر؛ مع التقليل من فقدان المتابعة من خلال ربط الفحص بالعلاج في أقل قدر ممكن لات من الزيارات (6 – 9)
يقى النوعان المتوافران حديثاً من اللقاحات من الإصابة بالأنماط عالية الخطورة لفيروس الورم الحُليمي البشري وهي الأنماط (١٦ , ١٨). كما يقيان أيضا من الأمراض المرتبطة بهذه الأنماط .(10- 11) تشير نتائج التجارب الإكلينيكية المستمرة إلى كفاءة عالية في الوقاية من الإصابة بالالتهابات وكذلك من إصابات ما قبل التسرطن في عنق الرحم بين الفتيات والنساء اللاتي لم يصبن من قبل بهذه الأنماط عند وقت أخذ اللقاح. ولما كان معدل النجاح أكثر إنخفاضًا بين من تعرضن بالفعل للإصابة بالفيروس الحليمي البشري؛ فقد انصب التركيز على الفتيات في سن المراهقة باعتبارهن المجموعة المستهدفة ذات الأولوية. أحد العوائق الأكثر وضوحًا أمام البلدان النامية هي سعر اللقاح، حيث تقدر تكلفة سلسلة الجرعات الثلاث من اللقاح الذي تنتجه شركة ميرك بحوالي ٣٦٠ دولاراً في الولايات المتحدة، وحتى مع تعدد مستويات التسعير فمازالت الأسعار تتعدى إمكانات الدول النامية. أعلن المصنعون عن استعدادهم لتوفير اللقاح بتكلفة أقل من أجل البلدان النامية، ولكن هذه الأسعار ليست معلومة بعد.
الوقاية من سرطان عنق الرحم: قرارات صعبة
تتطلب إضافة لقاح جديد لبرنامج التطعيم الوطنى أن يوضع في الاعتبار العبء الممكن تجنبه، والقيمة النسبية للقاح مقارنة بالاستخدامات البديلة للموارد، ومدى القدرة على شرائه ، واحتمالية قبول الجمهور به، والبعد السياسي في دعم لقاح ضد مرض ينتقل عبر الاتصال الجنسي، وكذلك مدى إمكانية تحقيق تغطية كبرى بين الفتيات في سن المراهقة. وتزداد المسألة تعقيدًا عند محاولة الجمع بين استخدام المسوح الواسعة وتقديم اللقاح. فكل منهما يتم مع مجموعات عمرية مختلفة، ويتطلبان موارد مالية قد تأتي من مصادر مختلفة، والتحديات العملياتية لكل منهما متفردة، كما يتباين اعتماد كل منهما على البنية التحتية القائمة؛ ومن ثم فإن تحقيق تغطية واسعة لكل منهما قد تتباين جدواه على نحو كبير فيما بين البلدان وداخل كل بلد.
إن توقع أثر برنامج الوقاية من مرض سرطان عنق الرحم على مستوى السكان أمر شديد التعقيد؛ حيث تمتد الفترة الزمنية بين العدوى وظهور المرض إلى عدة عقود، كما أن أفضل البيانات المتوافرة تقوم على النقاط النهائية الوسيطة، وتستهدف خيارات الوقايتين الأولية والثانوية مكونات غاية في الاختلاف من المرض، بالإضافة إلى أن التجارب الضابطة باستخدام عينات عشوائية ليست مجدية وليست أخلاقية.(12 – 14) ويمكن للنماذج الرياضية القائمة على الكمبيوتر أن تمثل أدوات مفيدة في التغلب على هذه التحديات، حيث توفر إطاراً منهجيًا لتركيب البيانات بأسلوب متسق داخليًا ومقبول من حيث المعطيات الوبائية.(8, 12, 14, 15)
يحتاج صُناع القرارات إلى معلومات حول القيمة النسبية للإستثمارات في اللقاح مقابل المسوح، وأوجه التقوية التي قد تتحقق بالجمع بين النموذجين، وكذلك “أفضل الرهانات” للوصول إلى برنامج مستدام للوقاية من مرض سرطان عنق الرحم. علاوة على ما تقدم فإ توصيات سياسة التطعيمات الصادرة عن منظمة الصحة العالمية، وآليات تنسيق التمويل مثل الاتحاد العالمي للقاحات والتطعيمات والصندوق الدوار لمنظمة الصحة الأمريكية تتطلب معلومات حول التكلفة المالية المطلوبة ومردود تكلفة تلقى الشابات للقاح لفيروس الحليمي البشري (۱٦ , ۱۸). واستجابة لهذه الإحتياجات أجرينا سلسلة من التحليلات ركزت على تقييم تلقي الفتيات للقاح الفيروس الحليمي البشري (16, 18) في البلدان منخفضة ومتوسطة الدخول. (16 – 22) توجز هذه الورقة أهم الخصائص التي أبرزتها التحليلات التي ركزت على الدول المؤهلة (72 دولة) للتعامل مع الإتحاد العالمي للقاحات والتطعيمات و ٣٣ من بلدان أمريكا اللاتينية ومنطقة الكاريبي.
المقاربة المنهجية
علم اتخاذ القرار وتحليل مردود التكلفة
استندنا في مقاربتنا التحليلية على علم إتخاذ القرار، وهو فرع من المعرفة يوفر أسلوباً بنيويًا منطقياً ليتيح لعملية أخذ القرارات المعقدة خيارات أو بدائل عديدة، ومقايضات حتمية وكذلك عدداً من الرؤى الممكنة. ويتأصل في النهج التحليلي للقرار تركيز واضح على تحديد نتائج القرارات أو تبعاتها وقياسها وتقييمها، وفي الوقت نفسه طرح الشكوك المحيطة بهذه النتائج وقت اتخاذ القرارات، أن تندرج هذه العناصر ضمن نموذج لتنظيم مشكلة اتخاذ القرار مع مرور الوقت. وبينما قد يتم اختيار أنواع مختلفة من النماذج للتعامل مع تعقيد مشكلة القرار إلا أنها جميعًا تعتمد على التحليل الرياضي لمقارنة أداء البدائل.(23)
تحليل مردود التكلفة هو نوع محدد من تحليل القرارات، تقارن بشكل منهجى العلاقة بين التبعات الإقتصادية بسبب التدخلات الصحية المختلفة وما تؤدى إليه من تحسن فى الصحة. يتناول تحليل مردود التكلفة أوجه السؤال التالي: “ما حجم التحسن في الصحة المقدر تحقيقه، مقابل كل دولار ينفق على أي تدخل صحى مقارنة بعائد استخدام الموارد نفسها في أنشطة بديلة؟” (14، 24) إن المبدأ الضمني الموجه لتقييم الموارد في تحليل مردود التكلفة هو تكلفة الفرصة، والتي تعكس تنافس المطالب المجتمعية
شكل 1: تكاليف مكونات اللقاح

يشير الرسم إلى ثلاث فرضيات حول التكلفة وفقاً لجرعة لقاح فيروس HPV16، 18
يتطابق طول الخط الرأسى مع إجمالى التكلفة وفقاً للمرأة المتلقية للقاح (۲٥ دولار عالمی و 50 دولار عالمی و75 دولار عالمى)، كما تمثل الأقاليم المظللة تكاليف المكونات.
على موارد محدودة. يوصف آداء التدخلات البديلة الخاضعة للمقارنة في التحليل من خلال استخدام الزيادة في نسب مردود التكلفة، وتعرف هذه النسب بأنها التكلفة الإضافية لإستراتيجية محددة مقسومة على ميزتها الإضافية، مقارنة بالإستراتيجية الفضلى التالية.
في التحليلات المعروضة هنا تقدر التكاليف بالدولار العالمي السائد، وهي العملة المستخدمة لترجمة قياسات التكلفة بعملة دولة ما إلى عملة شائعة (الدولار الأمريكي)، لتعكس الاختلافات في مستويات الأسعار بين البلدان. (25, 26) والدولار العالمي له القوة الشرائية نفسها للدولار الأمريكي في الولايات المتحدة. ولكي يمكن المقارنة بين التدخلات المختلفة في مجال الصحة العامة، تعدد الفوائد: الزيادة المكتسبة في العمر المتوقع، وعدد وفيات السرطان التي تم توّقيها، بالإضافة إلى عدد سنوات العمر معدلة حسب الإعاقة التي تم تجنبها. (عدد سنوات العمر المعدلة حسب الإعاقة DALYS هي وحدة لقياس الصحة المفقودة نتيجة لمرض ما، مع الأخذ في الاعتبار كل من الوفاة المبكرة، وتأثر نوعية سلبًا الحياة بسبب الإعاقة).(27)
ما من معيار عالمي يعرف المعدل الحدّى لمردود التكلفة، والذي يعتبر التدخل جيدًا من منظور مردود التكلفة إذا كان أدنى منه. والقاعدة الشائعة، وفقًا لتقرير “لجنة الاقتصاد الكلي والصحة“، هي أن التدخلات تعتبر “ذات مردود عإلى للتكلفة” إذا ما اتسمت بمعدلات لمردود التكلفة أقل من نصيب الفرد في الناتج الإجمالي المحلي.(25, 26, 28) ويمكن لإستراتيجية لقاح فيروس الورم الحُليمي البشري (۱٦ , ۱۸) أن تصل بالفعل “للمعدل الحدي” الأكثر انخفاضًا، والمطلوب للمنافسة على الموارد النادرة إذا ما كانت معدلات مردود التكلفة للقاحات الموجودة (مثل تطعيمات الأطفال) أقل بكثير من الناتج الإجمالي المحلي، كما في القاعدة المشار إليها أعلاه. (14)
نظرة عامة تحليلية
باستخدام البيانات السكانية من ٧٢ دولة مؤهلة من الاتحاد العالمي للقاحات والتطعيمات و ٣٣ من بلدان أمريكا اللاتينية ومنطقة الكاريبي، جنبًا إلى جنب مع البيانات الوبائية في الدولة أو الإقليم أو الاثنين معًا، تم تخدام مقاربة نموذجية لتقدير تأثير التلقيح ضد فيروس الحُليمي البشري (١٦ , ۱۸) على تجنب حالات السرطان سريع الانتشار، ووفيات السرطان، ومكاسب العمر المتوقع، وعدد سنوات العمر المعدلة وفقًا لتأثير الإعاقة، والمعدلات الإضافية لمردود التكلفة (دولار عالمی / عدد سنوات العمر المعدلة وفقًا لتأثير الإعاقة). ويمكن الاطلاع على الوثائق المتعلقة بتطوير النموذج، ومصادر البيانات، ومناهج دعم تحليل البيانات والتركيبات ولاسيما الإفتراضات التحليلية، في النشرات الحديثة وملحقاتها ذات الصلة (16 – 22, 29 – 31) افترض التحليل أن إعطاء اللقاح للفتيات دون الثانية عشر (قبل التعرض للاتصال الجنسي) سيكون فعالاً في الوقاية من فيروس الحُليمي البشرى (١٦ , ۱۸) إذا ما استخدمته فتيات بدون إصابات سابقاً وأنه يعطى تحصينًا من الفيروس على مدى الحياة. لقد التزمنا بتوجيهات إرشادية موحدة من أجل التقييم الاقتصادي.(24 , 26 – 28 ) قیمت تحلیلات الحساسية كيف يمكن للمؤشرات غير الثابتة (مثل فعالية اللقاح) والافتراضات (مثل مستويات تغطية التطعيم) أن تؤثر على النتائج.
بما أن سعر اللقاح وتكاليف تقديمه للبلدان منخفضة ومتوسطة الدخول غير مؤكدة حاليًا؛ فقد حددنا قيمة مجمعة “للتكلفة لكل فتاة تلقت اللقاح“. تم تصنيف هذه القيمة المجمعة وفقًا لتكاليف اللقاح، والفاقد والشحن والتوريد، والجوانب الإدارية، والتكاليف البرنامجية فضلاً عن دعم نظام التطعيم.( 17, 32, 33) على سبيل المثال توازي تكلفة ٢٥ دولاراً عالمياً لكل فتاة تتلقى اللفاح ثلاث جرعات من اللقاح بمبلغ ٥ دولارات كل منها، و ٢.٢٥ دولار للمفقود منه، و 1.31 دولار لشحنة وتوريده و1.50 دولار لأخذه و ٤.٩٤ دولار لدعم نظام التطعيم والتكاليف البرنامجية (الشكل 1)(17) في البلدان التي تم فيها تحليل استراتيجيات الفحص، أدرجت أيضًا التكاليف الطبية المباشرة (مثل فريق العمل والإمدادات والمعدات ونقل العينات) والتكاليف البرنامجية، ووقت المرأة وتكاليف الانتقال. (7, 16, 34)
يشير الرسم إلى ثلاث فرضيات حول التكلفة وفقًا لجرعة لقاح فيروس الورم الحُليمي البشري (16, 18) (٥ دولارات و ۱۲.۲5 دولار و19.50 دولار). يتطابق طول الخط الرأسي مع إجمالي التكلفة وفقًا للمرأة المتلقية للقاح (۲5 دولاراً عالمياً و 5۰ دولاراً عالمياً و ٧٥ دولاراً عالمياً). كما تمثل الأقاليم المظللة تكاليف المكونات المختلفة منها (1) ثلاث جرعات من اللقاح والمفقود منه و(۲) توريدات اللقاح (المفقود من المورد والشحن) و(۳) أخذ اللقاح و(٤) دعم نظام التطعيم.
النتائج والرؤى
إلى أي درجة من المتوقع أن تنخفض حالات سرطان عنق الرحم مع أخذ لقاح فيروس الحليمي البشري في سن المراهقة؟
مع افتراض تغطية بنسبة %۷%، فإن الحد الوسطي لمخاطر السرطان على مدى الحياة قد انخفض بنسبة ٤٠ – ٥٠% بينما جاء أقل من ٤٠% في بعض البلدان (مثل نيجيريا وغانا وتشيلي) وأعلى من ٥٠% في بلدان أخرى (مثل الهند وأوغندا والأرجنتين). تأثر الانخفاض المطلق لسرطان عنق الرحم في كل بلد بمدى حدوث سرطان عنق الرحم، وهيكل أعمار السكان، وتغطية اللقاح، بينما اعتمد الانخفاض النسبي على الجزء الخاص بالسرطان الناتج معة عن أنماط فيروس الحًليمي البشري (16, 18) (17)
ارتباط الفحص الجماعي باللقاح قلل من خطر سرطان عنق الرحم الناتج عن أنماط فيروس الحليمي لأخذه البشري غير التي يستهدفها اللقاح، وذلك بالإضافة إلى أنماط (16, 18). على سبيل المثال، مع افتراض تغطية تبلغ 70% في تشيلي جاء الإنخفاض في نسبة خطر السرطان يببلغ 25% إضافية، نتيجة المسح ثلاث مرات على مدار الحياة (مثال ٣٥ و ٤٠ و ٥٠ عاماً)، والذي جرى على النساء اللائي تلقين اللقاح في فترة المراهقة (الرسم ٢). أظهرت التحليلات في بلدان أخرى نتائج مماثلة، مع تفاوت في مقدار الفائدة المضافة وفقًا لكفاءة اختبار المسح ومدى تكراره وتغطيته.(8)
شكل2: متوسط انخفاض خطر سرطان عنق الرحم على مدى الحياة في تشيلي
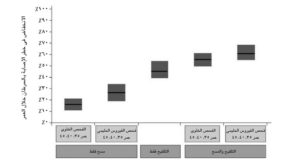
يمثل هذا المدى الحد الأدنى والحد الأقصى من الانخفاضات المحققة بتغطية تبلغ 70% لكل استراتيجية باستخدام تحليل الحساسية الاحتمالية، ويمثل الخط السميك الانخفاض المتوسط المحقق.
-
هل من الممكن إنقاذ المزيد من النساء باستهداف البلدان ذات المعدلات الأعلى في الإصابة بالسرطان؟
كانت الأعداد المطلقة للوفيات في البلدان ذات المعدلات الأعلى للإصابة بسرطان عنق الرحم (الإصابة بالمرض معدلة حسب العمر لكل 100.000 شخص تكون سنوات التعرض للخطر أكبر من۳۲.٦) أقل منها في البلدان ذات المعدلات المتوسطة من الإصابة بسرطان عنق الرحم وذات الكثافة السكانية الكبيرة. وفي الواقع ما بين البلدان ٧٢ المؤهلة من الاتحاد العالمي للقاحات والتطعيمات، مثلت البلدان ذات معدلات الإصابة الأعلى أقل من ٢٥% من حالات الوفيات المتجنبة بينما مثلت البلدان ذات معدلات الإصابة الأقل ۱۰% (الشكل3، الجزء الأعلى). ستصل تقريبًا نسبة الوفيات المتجنبة بمنطقة جنوب شرق آسيا لمنظمة الصحة العالمية حوالي ٥٧%، حيث توجد ٤١% من هذه النسبة في الهند وحدها. كما ستبلغ النسبة في بلدان أفريقيا ٣٠% إضافية.(١٧) وبالمثل، في بلدان أمريكا اللاتينية ومنطقة الكاريبي (۳۳ بلدًا) مثلت البلدان ذات الحد الأقل من خطر السرطان (نسبة الإصابة بالمرض معدلة حسب العمر أكبر من 26.1) نسبة 45% من الوفيات المتجنبة (الشكل3، الجزء السفلي). حوالي 71% من الوفيات المتجنبة ستكون بأمريكا الجنوبية و ٢٣% في أمريكا الوسطى و6% في منطقة الكاريبي.(18)
-
كم من النساء يمكن إنقاذ حياتهن من خلال برنامج يقوم بتطعيم ٧٠% من الفتيات البالغات ١٢ عامًا خلال ١٠ سنوات متتالية؟
سيتم تجنب ما يقرب من ثلاثة ملايين حالة وفاة ما بين النساء اللائي تلقين اللقاح في سن المراهقة بالبلدان ۷۲ المؤهلة من الاتحاد العالمي للقاحات والتطعيمات(17) ولقد أدى تطبيق برنامج مماثل في ٣٣ دولة بأمريكا اللاتينية ومنطقة الكاريبي إلى تجنب ما يزيد على مليون سيكون حالة إضافية من سرطان عنق الرحم. (18) ولقد رصدنا في مكان آخر سيناريوهات أخرى للتوسع تأخذ في الاعتبار التكاليف الافتراضات الخاصة بالدولة (نصيب الفرد من إجمالي الدخل القومي، وتغطية الجرعات الثلاث للتطعيم الثلاثي (الدفتريا، السعال الديكي والتيتانوس)، ونسبة الفتيات المسجلات في الصف الخامس الإبتدائي) من أجل البدء في استخدام اللقاح ومعدل التوسع، والتغطية الممكن تحقيقها.(17)
-
هل سيتسم لقاح فيروس الحليمي البشري (١٦ ، ١٨) للفتيات في سن المراهقة بمردود التكلفة؟
يمكن أن يتسم لقاح فيروس الحليمي البشري (١٦ , ۱۸) بمردود تكلفة مرتفعة. وتكون قيمته مقاربة لقيمة اللقاحات الجديدة؛ حتى في البلدان الأكثر فقرًا شريطة أن للحـ تكون تكلفة تلقي الفتاة للقاح أقل بكثير من السعر الحالي في البلدان المتقدمة. في البلدان المؤهلة من الاتحاد العالمي اللقاحات والتطعيمات (۷۲ بلداً) – والتي تستخدم معيار أن يكون معدل مردود التكلفة أقل من نصيب الفرد من الناتج الإجمالي المحلي – اتسم مبلغ ۱۰ دولارًا عالمية للفتاة المتلقية للقاح (۲.۰۰ دولار للجرعة مع افتراض الحصول على الجرعات الثلاث، بالإضافة إلى المفقود منه وأخذه ودعم البرنامج) بمردود تكلفة جيدة جدًا (شكل ٤ – الجزء الأعلى).(17) وفي منطقة أمريكا اللاتينية والكاريبي (۳۳ دولة) ويمبلغ ٢٥ دولارًا عالمي للفتاة المتلقية للقاح (٥ دولارات للجرعة). جاءت التكلفة حسب عدد سنوات العمر المعدلة وفقًا لتأثير الإعاقة أقل من ٤٠٠ دولار عالمي (الشكل ٤ – الجزء السفلي).(18) تمثل هذه النسبة ليس فقط قيمة جيدة للموارد – حيث إنها أقل من نصيب الفرد من الناتج المحلي الإجمالي في كل دولة – ولكن المقارنة بينها وبين النسب الخاصة باللقاحات الجديدة ستكون لصالحها أيضًا. (25, 28) على سبيل المثال تتراوح مردود التكلفة للقاح المُكوَّرات الرئوية بين ١١٠ –٢.٥٠ دولار بين الكثير من البلدان، والأمر نفسه مع لقاح فيروس الروتا، حيث تترواح مردود التكلفة بين 290 دولارًا و ۱۲.۳۰۰ دولار في بلدان أمريكا اللاتينية. (18)
-
حتى وإن اتسم اللقاح بمردود التكلفة هل سيكون في متناول اليد؟
على الرغم من ميل الكفة نحو مردود التكلفة فإن تقييم التكاليف العالية المطلوبة على المدى القريب آثار المخاوف بشأن مدى إمكانية شراء اللقاح (الشكل ٤). على سبيل المثال تفاوتت المتطلبات المالية لتلقي الفتيات البالغات ١٣ عاماً من العمر للقاح في البلدان ۷۲ المؤهلة من الاتحاد العالمي للقاحات والتطعيمات، وفقًا لمعدلات الزيادة الخاصة بكل دولة لمدة عشر سنوات، من حوالي ۹۰۰ مليون دولار (۲ دولار للجرعة – ١٠ دولارات عالمية لكل فتاة تلقت اللقاح) إلى ما يزيد على 4 مليارات دولار (۱۲.۲5 دولار للجرعة – ٥٠ دولار عالمياً لكل فتاة تلقت اللقاح).(17) وفي البلدان أمريكا اللاتينية ومنطقة الكاريبي (۳۳ بلدًا) وصلت تكلفة اللقاح لنسبة 70% من الفتيات البالغات ١2 عاماً لمدة خمس سنوات على التوالي ٣٦٠ مليون دولار (٥ دولارات للجرعة) ولكن تعدت التكلفة ١.٢٥ مليار دولار إذا زاد ثمن الجرعة إلى ١٩.٥٠ دولار للجرعة. (18)
-
هل هناك أية مزايا أخرى بالإضافة إلى الوقاية من وفيات سرطان عنق الرحم؟
باستخدام بيانات من ٧٢ دولة حول متوسط معدل الخصوبة، وحجم السكان وفقًا للعمر، والأنماط العمرية لوفيات سرطان عنق الرحم، خرجنا بالتقدير التالي: أنه الجزء من خلال برنامج تطعيم مدته عشر سنوات وبتغطية تبلغ ٧٠% سوف يتم تجنب فقدان الأم بسبب سرطان عنق الرحم لحوالي ١٠ ملايين طفل، وما بين 1.5 ملیون و ۲.۹ مليون من هؤلاء الأطفال سيكونون دون الثامنة عشر. (17) وباستخدام البيانات الخاصة بمعدل الرواتب من منظمة العمل الدولية (35) قمنا بتطبيق المناهج المشار إليها آنفًا، في ثلث البلدان فقط حيث توفرت البيانات بسهولة، لتوفير رؤية عامة حول تكاليف الإنتاجية المرتبطة بالوفاة المبكرة بسبب سرطان عنق الرحم عند تقييم العمل (بما فيها العمل المنزلي ) الذي تقوم به النساء اللاتي سيفقدن حياتهن بسبب هذا المرض، وجدنا أن العوائد المستقبلية المفقودة هنا (أي تكاليف الإنتاجية) تعدت مبلغ ٢ مليار دولار.
شكل3: توزيع حالات وفيات السرطان المتجنبة
البلدان المؤهلة من الإتحاد العالمي للقاحات والتطعيمات (72 بلدًا)
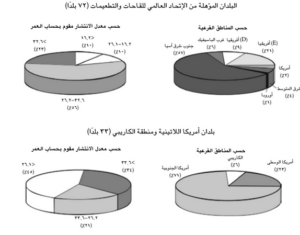
-
توزيع حالات وفيات السرطان المتجنبة من خلال تطعيم الفتيات في سن المراهقة في البلدان ٧٢ المؤهلة من الإتحاد العالمي للقاحات والتطعيمات (الجزء العلوي) والبلدان ٣٣ لأمريكا اللاتينية ومنطقة الكاريبي (الجزء السفلي) مقسمة حسب حدوث السرطان (اليسار) والمنطقة الجغرافية (اليمين)
-
مناطق منظمة الصحة العالمية أفريقيا، والأمريكتين، ومنطقة البحر المتوسط الشرقية، وأوروبا، وجنوب شرق آسيا، وجنوب الباسيفيكي
-
“D” تشير إلى نسبة وفيات مرتفعة بين الأطفال والكبار، و“E” تشير إلى نسبة وفيات مرتفعة بين الأطفال ومرتفعة للغاية بين الكبار
لقاح الفيروس الحليمي البشري (۱٦ ، ۱۸) للمراهقات في البلدان المؤهلة من الاتحاد العالمي للقاحات والتطعيمات (۷۲ بلدًا) بتكلفة تبلغ ٢ دولار للجرعة (الشكل الماسي) و5 دولارات (الشكل الدائري) و ۱۲.۲5 (شكل المثلث) وهي التكلفة المقابلة لمبلغ ۱۰ دولار عالمياً و ٢٥ دولار عالمياً و٥٠ دولاراً عالمياً على التوالي لكل فتاة تلقت اللقاح.
برامج لقاح فيروس الحليمي البشري (١٦، ١٨) للفتيات في سن المراهقة في بلدان أمريكا اللاتينية ومنطقة الكاريبي (۳۳ بلدًا) بتكلفة للجرعة تبلغ ٥ دولارات (يسار) و ۱۲،۲5 دولار (وسط) و ۱۹.5۰ دولار (يمين) بما يعادل. ٢٥ دولاراً عالمياً و ٥٠ دولاراً عالمياً و ٧٥ دولاراً عالمي على التوالي لكل فتاة تلقت اللقاح.
-
كيف تقارن الفوائد المتوقعة من لقاح فيروس الحليمي البشري (١٦، ١٨) مع فوائد اللقاحات الجديدة؟
مع الأخذ في الاعتبار البلدان المؤهلة من الإتحاد العالمي للقاحات والتطعيمات، يتم تجنب ١٣ حالة وفاة بسبب سرطان عنق الرحم لكل ۱۰۰۰ فتاة تلقت اللقاح، أما
شكل ٤ أ مردود التكلفة مقابل القدرة على الشراء البلدان ٧٢ المؤهلة من الاتحاد العالمي للقاحات والتطعيمات
القيمة المالية بالدولار الأمريكي

لقاح الفيروس الحليمي البشري ( 16, 18) للمراهقات في البلدان المؤهلة من الاتحاد العالمي للقاحات والتطعيمات (۷۲ بلدًا) بتكلفة تبلغ ٢ دولار للجرعة (الشكل الماسي) و5 دولارات (الشكل الدائري) و 12.25 (شكل المثلث) وهي التكلفة المقابلة لمبلغ ١٠ دولار عالميًا و ٢٥ دولار عالميًا و 50 دولاراً عالمياً على التوالي لكل فتاة تلقت اللقاح.
شكل ٤. ب: بلدان أمريكا اللاتينية ومنطقة الكاريبي (۳۳ بلدًا)

برامج لقاح فيروس الحليمي البشري (, 18) للفتيات في سن المراهقة في بلدان أمريكا اللاتينية ومنطقة الكاريبي (۳۳ بلدًا) بتكلفة للجرعة تبلغ 5 دولارات (يسار) و12.25 دولار (وسط) و 19.50 دولار (يمين) بما يعادل ٢٥ دولارًا عالميًا و ٥٠ دولارًا عالميًا و ٧٥ دولاراً عالمي على لتوالي لكل فتاة تلقت اللقاح.
بين البلدان الأفقر في أفريقيا فيتم تجنب ۱۷ حالة وفاة لكل ١٠٠٠ فتاة تلقت اللقاح. (17) في بلدان أمريكا اللاتينية ومنطقة الكاريبي كان متوسط عدد حالات الوفيات المتجنبة ٢٧ حالة لكل ١٠٠٠ فتاة تلقت اللقاح في المنطقة برمتها، بينما ارتفع هذا الرقم في الأقاليم مرتفعة الخطر (مثال ٤١ حالة وفاة متجنبة لكل ١٠٠٠ فتاة تلقت اللقاح في هايتي و ۳۲ حالة وفاة متجنبة لكل ١٠٠٠ فتاة تلقت اللقاح في تشيلي).(18) تأتي النتيجة في صالح لقاح فيروس الورم الحُليمي البشري عند المقارنة بالتقارير التقديرية لثلاث حالات وفاة متجنبة لكل ١٠٠٠ طفل تلقى لقاح فيروس الروتا(38) و ٦.٨ حالة لكل ۱۰۰۰ طفل تلقى لقاح المُكورَّات الرئوية في البرازيل و 2.2 حالة لكل ۱۰۰۰ طفل تلقى اللقاح في تشيلي و ۲.۹ حالة لكل ۱۰۰۰ طفل تلقي اللقاح في أورجواي.(39)
-
ما هي الافتراضات غير المؤكدة التي كان لها عظيم الأثر على النتائج؟
بالنسبة للقاح الفتيات في سن المراهقة اعتمد استفادة عموم السكان بشكل كبير على عمر والعمر عند الاصابة بسرطان عنق الرحم، ونسبة الإصابة بالسرطان بسبب فيروس الحليمي البشري (۱٦ , ۱۸)، والتغطية المتحققة للفتيات في سن المراهقة. كما كانت فترة المناعة مثلاً من الأمور غير المؤكدة بشأن اللقاح؛ الأمر الذي كان من العوامل من المؤثرة أما أكثر العوامل تأثيرًا من زاوية مردود التكلفة فكان سعر اللقاح، والتكلفة البرنامجية المتعلقة ببرنامج تطعيم الفتيات في سن المراهقة. كانت نتائج مردود التكلفة أقل إيجابية إذا ما انخفضت التكاليف المرتبطة بسرطان عنق الرحم الانتشاري بنسبة ٥٠% أو إذا ما كانت الجرعات الأكبر المنشطة مطلوبة لإعطاء تحصين مدى الحياة.
لا تظهر حالات وفيات السرطان المتجنبة، ما بين الفتيات المتلقيات للقاح فيروس الورم الحُليمي البشري في سن المراهقة، إلا بعد مرور عقود على دفع تكاليف اللقاح، بينما بالنسبة للقاحات الأخرى (مثل لقاح فيروس الروتا) تظهر النتائج الصحية والإقتصادية بعد فترة قصيرة. من ثم فإن توقف التكلفة في المستقبل والفوائد المستقبلية – والمطلوبة لتوحيد عمليات التقييم الإقتصادية المتعلقة بالصحة العامة – (14, 24, 40) أكثر تأثيرًا بالنسبة للقاح فيروس الحُليمي البشري عنها بالنسبة للقاحات الأطفال. على سبيل المثال سوف تنخفض معدلات مردود التكلفة بدون وقف المزايا بنسبة ٨٠% (أي تكون أكثر جذبًا).(17, 18)
وقد نشرت في السابق تحليلات الحساسية، التي تتحري تأثير قياسات مدخلات النموذج وافتراضاته التقديرية وشكوكه الرئيسية، في كل من البرازيل وفيتنام والهند.(16، 21، 22) فضلاً عن العديد من البلدان الأخرى.(7, 8, 12, 14, 17 – 19, 41)
تشير نتائجنا العامة إلى أن توفير لقاح لفيروس الورم الحُليمي البشري (16, 18) لنسبة ٧٠% من الفتيات الشابات في سن المراهقة، في البلدان الأكثر فقرًا والمؤهلة من الإتحاد العالمي للقاحات والتطعيمات (۷۲ بلد)؛ من الممكن له أن يحول دون الوفيات المستقبلية لنحو ثلاثة ملايين امرأة تتلقى اللقاح خلال العقد المقبل ومع إضافة بلدان أخرى غير المؤهلة من الاتحاد العالمي للقاحات والتطعيمات، من أمريكا اللاتينية ومنطقة الكاريبي، علاوة على الصين وتايلاند ۱۹ ، سوف يمنع ذلك من حدوث وفيات مستقبلية أخرى تبلغ حوالي مليون حالة. من منظور عالمي تمثل البلدان المعرضة لأكبر خطر للإصابة بالسرطان أقل من ثلث حالات الوفيات المتجنبة المتوقعة، وهو الأمر الذي يلقي بالضوء على أهمية اتباع لقة منهج إقليمي عالمي للقاح حيث إنه سيكون الأكثر فاعلية في الحد من العبء العالمي الكلي. في الواقع كان الرقم الأكبر المتوقع لحالات الوفيات الممكن تجنبها ضمن البلدان التي بها ظهور متوسط لسرطان عنق الرحم، ولكن التي بها نسبة سكان كبيرة.
لابد أن تكون التكاليف السنوية للدافع (أي القدرة على الشراء) وقياس مردود التكلفة (أي قيمة النقود)، وهي الأمور المتعلقة باللقاح، مشجعة حيث أنها ستتنافس على الدولارات مع برامج التطعيم الموجودة بالفعل ومبادرات التوسع واللقاحات الأخرى الجديدة؛ (42) وبالطبع سيكون سعر اللقاح محددًا رئيسيًا لهذين البُعدين. وحتى إذا كانت التكلفة أكثر ارتفاعًا بدرجة ما من اللقاحات التقليدية، تعتمد شريطة أن لا تتعدى تكلفة تلقي الفتاة للقاح ١٠ دولار – 25 دولارًا، ستكون مردود التكلفة للقاح فيروس البشري الموت الحليمي (16, 18) للفتيات في سن المراهقة إيجابية، حتى في البلدان الفقيرة نسبيًا. ولكى يكون اللقاح في متناول اليد لابد من تخفيض الأسعار الحالية للقاح، بالإضافة إلى توفير آليات فعالة تتمتع بمردود التكلفة للوصول إلى تغطية واسعة للفتيات في سن المراهقة. على سبيل المثال حدد البنك الدولي أمريكا اللاتينية باعتبارها واحدة من أكثر منطقتين في العالم تتسمان بعدم المساواة في توزيع الدخول (43) ومع افتراض تكلفة مقاربة للسعر الحالي للقاح في البلدان المتقدمة (۱۲۰ دولاراً للجرعة) تتراوح مردود التكلفة الخاصة بهذا اللقاح في هذه المنطقة بين 2.400 دولار وما يزيد على 10.000 دولار، لتتعدى بذلك بشكل كبير المعدلات المرتبطة بلقاحات الأطفال.(18) وعلاوة على ذلك، سوف تبلغ الآثار المالية لفترة خمس سنوات فقط من تلقي اللقاح بهذه التكلفة ٦.٣٨ مليار دولار تقريبًا في بلدان أمريكا اللاتينية، وذلك مقارنة بمبلغ ۸۱۱ مليون دولار إذا كان السعر ١٢.٢٥ دولار للجرعة الواحدة.
إن الاحتمالات المستقبلية لتقديم لقاحات فيروس الحُليمي البشري بالاقتران مع برنامج لتطعيم الفتيات في سن المراهقة من الممكن له أيضًا أن يوفر الفرص لتقوية أنظمة الصحة، وذلك من خلال وضع آليات جديدة لتقديم اللقاح ورصد الأثر. إذا ما نجح ذلك، فقد يُيسر تقديم خدمات صحية أخرى للفتيات في سن المراهقة، مثل تطعيم التيتانوس وتقديم الاستشارات حول السلوكيات الجنسية الخطرة.(44) توجد حاجة إلى بيانات خاصة بكل دولة باستخدام أدوات معيارية للتسعير، وذلك لتقييم الخيارات البديلة المتاحة فيما يتعلق بالبرامج وتقديم اللقاح، والتكاليف المرتبطة بالتوسع، فضلاً عن الأبعاد الاقتصادية المرتبطة بالتوسع في البرامج الأخرى الموجهة للمجموعة العمرية في سن المراهقة.
يبقى أن نؤكد على أهم الفجوات المتعلقة بالأدلة؛ حيث تعتمد التوقعات القائمة على النموذج، في ما يتعلق بفوائد اللقاح على المدى الطويل على العديد من الافتراضات غير المؤكدة.(12, 15, 16, 20, 31, 41, 45)أن فترة المناعة الناجمة عن اللقاح على المدى الطويل، وضرورة تلقي جرعة منشطة، ومدى الحماية من السلالات المختلطة ومدتها ضد أنماط فيروس الحُليمي البشري الأخرى المكونة للورم والتي لا تتوفر في اللقاح، تظل جميعها أمورًا غير معروفة بعد. من الأمور الأخرى غير المؤكدة؛ مدى فاعلية اللقاحات بين الأماكن السائد فيها فيروس الحُليمي البشري بشكل كبير، ورد فعل أنماط فيروس الحليمي البشري الأخرى غير المستهدفة بعد تلقي اللقاح، وكذلك حجم المناعة الجماعية. لهذا يعتبر إجراء المزيد من الدراسات حول هذه القضايا أمراً يأتي في صدراة الأولويات.
بالنظر إلى كم الأمور غير المؤكدة الموجودة، وقصورات التحليلات القائمة على النموذج والتي من غير الممكن تجنبها، ينبغى التعامل مع الرؤى الناتجة ون عن هذه التحليلات على أنها تقديرات أولية للنتائج الصحية والاقتصادية للوقاية من سرطان عنق الرحم وفقًا للمعلومات المتوافرة الآن. إن القرارات على مستوى السياسة التي تواجهها البلدان منخفضة ومتوسطة الدخول، فيما يتعلق بتطبيق لقاح فيروس الحليمي البشري، وكيفية تطبيقه، هي قرارات معقدة، خاصة عندما نأخذ في الاعتبار أن الأفراد الذين سيستفيدون من هذا اللقاح لن يدركوا هذه الفوائد سوى بعد مرور سنوات عديدة. يمثل كل من العبء الممكن تجنبه ومردود التكلفة، والقدرة على الشراء، أبعاداً ثلاثة فقط من المعلومات الضرورية لاتخاذ القرارات بشأن تبني استخدام اللقاح. لكن هناك عدداً من المعايير المهمة بالقدر نفسه أيضاً، والتي ينبغي وضعها في الاعتبار مثل تأثيرات التوزيع والعدالة في التوزيع، والقدرة على تقديم اللقاح والحفاظ على التدخلات ذات الجودة، ومدى احتمال القبول الثقافي والدعم السياسي (14, 27, 42, 46)
لن يكون من السهل الوصول إلى تغطية واسعة النطاق للفتيات في سن المراهقة وكذلك التفاوض في الأسعار المقبولة وتأمين التمويل السريع للقاح. خلال فترة التأخير التقليدية والتى تستغرق عقودًا لجعل لقاح جديد متاحاً للبلدان الأكثر فقرًا، سوف تموت الملايين من النساء من مرض من الممكن تجنبه في ذروة أعمارهن. سوف يساعد في إنقاذ حياة النساء كل من الأمور الآتية: الالتزام العالمي بمواجهة التحديات المطلوبة لتوفير لقاح لفيروس الحليمي البشري (۱٦ , ۱۸) للفتيات في سن المراهقة في البلدان الأكثر فقراً، مع توفير خدمات وقاية ثانوية عالية الجودة للشابات من مرتين إلى ثلاث مرات على مدى الحياة. ورغم صعوبة تناول الموضوع بلغة الأعداد والنقود، فإن هذه الفوائد سوف تُترجم إلى عدد مساو من الأسر المعيشية والمجتمعات التي ستستفيد، وسيستفيد عدد أكبر من الأطفال الذين لن يفقدوا أمهاتهم بسبب سرطان عنق الرحم. بالنظر إلى الجهود المتزايدة لحشد موارد جديدة للتطعيم من خلال مبادرات مبتكرة لتمويل اللقاح، من الممكن لنتائج هذه التحليلات أن تحفز على الحوار المبكر وتدعمه بشأن قرارات الاستثمار في لقاح فيروس الحليمي البشري (١٦، ١٨).
1 -Parkin DM, Bray F. The burden of HPV-related cancers. Vaccine 2006;24(S3): S11–25.
2 -Muñoz N, Bosch FX, Castellsagué X, et al. Against which human papillomavirus types shall we vaccinate and screen? The international perspective. International Journal of Cancer 2004;111(2): 278– 85.
3 -Clifford G, Franceschi S, Diaz M, et al. HPV type-distribution in women with and without cervical neoplastic diseases. Vaccine 2006;24(S3):S26–34.
4 -Smith JS, Lindsay L, Hoots B, et al. Human papillomavirus type distribution in invasive cervical cancer and high-grade cervical lesions: a meta-analysis update. International Journal of Cancer 2007;121:621–32.
5 -Denny L, Quinn M, Sankaranarayanan R. Chapter 8: Screening for cervical cancer in developing countries. Vaccine 2006;24(S3):S71–77
6 -Goldie SJ, Kuhn LK, Denny L, et al. Policy analysis of cervical cancer screening strategies in low- resource settings: clinical benefits and cost-effectiveness. JAMA 2001; 285:3107–15.
7 -Goldie SJ, Gaffikin L, Goldhaber-Fiebert JD, et al. Cost-effectiveness of cervical cancer screening in five developing countries. New England Journal of Medicine 2005;353(20):2158–68.
8 -Goldie SJ, Kim JJ, Myers E. Chapter 19: Cost-effectiveness of cervical cancer screening. Vaccine. 2006;24(S3):S164–70.
9 -Sankaranarayanan R, Gaffikin L, Jacob M, et al. A critical assessment of screening methods for cervical neoplasia. International Journal of Gynaecological Obstetrics 2005;89(S2):S4–12
10 -Ault KA, Future II Study Group. Effect of prophylactic human papillomavirus L1 virus-like particle vaccine on risk of cervical intraepithelial neoplasia grade 2, grade 3, and adenocarcinoma in situ: a combined analysis of four randomised clinical trials. Lancet 2007;369:1861–68.
11 -Harper DM, Franco EL, Wheeler CM, et al. Sustained efficacy up to 4.5 years of a bivalent L1 virus-like particle vaccine against human papillomavirus types 16 and 18: follow-up from a randomised control trial. Lancet 2006;367(9518):1247–55.
12 -Garnett GP, Kim JJ, French K, et al. Chapter 21: Modelling the impact of HPV vaccines on cervical cancer and screening programmes. Vaccine 2006; 24(S3):S178–86.
13 -Goldie SJ. Chapter 15: Public health policy and costeffectiveness analysis. Journal of the National Cancer Institute Monograph 2003;(31):102–10.
14 -Goldie SJ, Goldhaber-Fiebert JD, Garnett GP. Chapter 18: Public health policy for cervical cancer prevention: the role of decision science, economic evaluation, and mathematical modeling. Vaccine 2006;24(S3):S155–63.
15 -Kim JJ, Brisson M, Edmunds WJ, et al. Modeling cervical cancer prevention in developed countries. Vaccine 2008;26(11): K76–K86.
16 -Goldie SJ, Kim JJ, Kobus K, et al. Cost-effectiveness of HPV16,18 vaccination in Brazil. Vaccine 2007;25(33):6257–70.
17 -Goldie SJ, O’Shea M, Campos NG, et al. Health and economic outcomes of HPV16,18 vaccination in 72GAVI-eligible countries. Vaccine 2008;26(32):4080–93.
18 -Goldie SJ, Diaz M, Constenla D, et al. Mathematical models of cervical cancer prevention in LatinAmerica and the Caribbean. Vaccine 2008;26 (S11):L59–72.
19 -Goldie SJ, Diaz M, Kim SY, et al. Mathematical models of cervical cancer prevention in the Asia Pacific region. Vaccine 2008; 26(S12):M17-29.
20 -Kim JJ, Andres-Beck B, Goldie SJ. The value of including boys in an HPV vaccination programme: a cost-effectiveness analysis in a low-resource setting. British Journal of Cancer 2007;97(9):1322–28.
21 -Kim JJ, Kobus KE, Diaz M, et al. Exploring the cost-effectiveness of HPV vaccination in Vietnam: insights for evidence-based cervical cancer prevention policy. Vaccine 2008;26(32): 4015–24.
22 -Diaz M, Kim JJ, Albero G, et al. Health and economic impact of HPV 16 and 18 vaccination and cervical cancer screening in India. British Journal of Cancer 2008;99(2):230–38.
23 -Kim SY, Goldie SJ. Cost-effectiveness analyses of vaccination programmes: a focused review of modeling approaches. Pharmacoeconomics 2008;26(3):191–215.
24 -Gold MR, Siegel JE, Russell LB, et al, editors. Cost-effectiveness in Health and Medicine. New York: Oxford University Press; 1996.
25 -World Health Organization. Macroeconomics and Health: investing in health for economic development: report of the commission on macroeconomics and health. Geneva: WHO; 2001.
26 -World Health Organization Statistical Information System. CHOICE (Choosing Interventions that are Cost Effective). At <www.who.int/choice/en/>. Accessed 29 January 2008.
27 -Evans DB, Edejer TT, Adam T, et al. Methods to assess the costs and health effects of interventions for improving health in developing countries. BMJ 2005;331(7525):1137–40.
28 -Disease Control Priorities Project (DCPP). At <www.dcp2.org/main/Home.html>. Accessed 28 January 2008.
29 -Goldhaber-Fiebert JD, Stout NK, Ortendahl J, et al. Modeling human papillomavirus and cervical cancer for analyses of screening and vaccination. Population Health Metrics 2007; 5(1):11.
30 -Kim JJ, Kuntz KM, Stout NK, et al. Multiparameter calibration of a natural history model of cervical cancer. American Journal of Epidemiology 2007; 166(2):137–50.
31 -Kim JJ, Goldie SJ. Health and economic implications of HPV vaccination in the United States. New England Journal of Medicine 2008;359(8):821-32.
32 -Kou U. Guidelines for estimating costs of introducing new vaccines into the national immunization system. Geneva: World Health Organization, Department of Vaccines and Biologicals; 2002., 2002.
33 -World Health Organization. Adding a vaccine to a national immunization programme: decision and implementation. WHO/IVB/05.18. 2005. At: <www.who.int/vaccinesdocuments/DocsPDF05/ 777_ screen.pdf>. Accessed 1 August 2008.
34 -Goldhaber-Fiebert JD, Goldie SJ. Estimating the cost of cervical cancer screening in five developing countries. Cost Effectiveness and Resource Allocation 2006;4:13.
35 -International Labour Organization. LABORSTA online database. At: <http://laborsta.ilo.org/>. Accessed 21 September 2008.
36 -Hu D, Bertozzi SM, Gakidou E, et al. The costs, benefits, and cost-effectiveness of interventions to reduce maternal morbidity and mortality in Mexico. PLoS ONE 2007; 2(1):e750.
37 -Max W, Rice DP, Sung HY, et al. Valuing human life: estimating the present value of lifetime earnings, 2000. (October 1, 2004). Center for Tobacco Control Research and Education. Economic Studies and Related Methods. Paper PVLE2000. At: http://repositories.cdlib.org/ctcre/esarm/PVLE2000/ Accessed
18 September 2008.
38 -IAVI/PATH. HPV vaccine adoption in developing countries: cost and financing issues. At: <http://www. iavi. org/viewfile.cfm?fid=47496>. Accessed 29 February 2008.
39 -Constenla D, Ortega-Barria E, Rheingans RD, et al. Economic impact of rotavirus vaccination in Panama. Anales de pediatría (Barcelona) 2008;68(2):128–35.
40 -Drummond MF, Sculpher MJ, Torrance GW, et al, editors. Methods for the Economic Evaluation of Health Care Programs. 3rd ed. New York: Oxford University Press; 2005.
41 -Goldie SJ, Grima D, Kohli M, et al. A comprehensive natural history model of HPV infection and cervical cancer to estimate the clinical impact of a prophylactic HPV-16/18 vaccine. International Journal of Cancer 2003;106(6):896–904.
42- Kim SY, Salomon JA, Goldie SJ. Economic evaluation of hepatitis B vaccination in low-income countries: using cost-effectiveness affordability curves. Bulletin of World Health Organization 2007;85(11):833–42.
43 -World Bank. Regional fact sheet. World Development Indicators 2008: Latin America and the Caribbean. At <http:// siteresources.worldbank.org/DATASTATISTICS/Resources/ lac_wdi.pdf>. Accessed 11 September 2008.
44 -Agosti JM, Goldie SJ. Introducing HPV vaccine in developing countries–key challenges and issues. New England Journal of Medicine 2007;356(19):1908–10.
45 -Haug CJ. Human papillomavirus vaccination – reasons for caution. New England Journal of Medicine 2008;359(8): 861–62.
46- Musgrove P, Fox-Rushby J. Cost-effectiveness analysis for priority setting. Disease Control Priorities in Developing Countries 2006; 271–83.
1 -Parkin DM, Bray F. The burden of HPV-related cancers. Vaccine 2006;24(S3): S11–25.
2 -Muñoz N, Bosch FX, Castellsagué X, et al. Against which human papillomavirus types shall we vaccinate and screen? The international perspective. International Journal of Cancer 2004;111(2): 278– 85.
3 -Clifford G, Franceschi S, Diaz M, et al. HPV type-distribution in women with and without cervical neoplastic diseases. Vaccine 2006;24(S3):S26–34.
4 -Smith JS, Lindsay L, Hoots B, et al. Human papillomavirus type distribution in invasive cervical cancer and high-grade cervical lesions: a meta-analysis update. International Journal of Cancer 2007;121:621–32.
5 -Denny L, Quinn M, Sankaranarayanan R. Chapter 8: Screening for cervical cancer in developing countries. Vaccine 2006;24(S3):S71–77
6 -Goldie SJ, Kuhn LK, Denny L, et al. Policy analysis of cervical cancer screening strategies in low- resource settings: clinical benefits and cost-effectiveness. JAMA 2001; 285:3107–15.
7 -Goldie SJ, Gaffikin L, Goldhaber-Fiebert JD, et al. Cost-effectiveness of cervical cancer screening in five developing countries. New England Journal of Medicine 2005;353(20):2158–68.
8 -Goldie SJ, Kim JJ, Myers E. Chapter 19: Cost-effectiveness of cervical cancer screening. Vaccine. 2006;24(S3):S164–70.
9 -Sankaranarayanan R, Gaffikin L, Jacob M, et al. A critical assessment of screening methods for cervical neoplasia. International Journal of Gynaecological Obstetrics 2005;89(S2):S4–12
10 -Ault KA, Future II Study Group. Effect of prophylactic human papillomavirus L1 virus-like particle vaccine on risk of cervical intraepithelial neoplasia grade 2, grade 3, and adenocarcinoma in situ: a combined analysis of four randomised clinical trials. Lancet 2007;369:1861–68.
11 -Harper DM, Franco EL, Wheeler CM, et al. Sustained efficacy up to 4.5 years of a bivalent L1 virus-like particle vaccine against human papillomavirus types 16 and 18: follow-up from a randomised control trial. Lancet 2006;367(9518):1247–55.
12 -Garnett GP, Kim JJ, French K, et al. Chapter 21: Modelling the impact of HPV vaccines on cervical cancer and screening programmes. Vaccine 2006; 24(S3):S178–86.
13 -Goldie SJ. Chapter 15: Public health policy and costeffectiveness analysis. Journal of the National Cancer Institute Monograph 2003;(31):102–10.
14 -Goldie SJ, Goldhaber-Fiebert JD, Garnett GP. Chapter 18: Public health policy for cervical cancer prevention: the role of decision science, economic evaluation, and mathematical modeling. Vaccine 2006;24(S3):S155–63.
15 -Kim JJ, Brisson M, Edmunds WJ, et al. Modeling cervical cancer prevention in developed countries. Vaccine 2008;26(11): K76–K86.
16 -Goldie SJ, Kim JJ, Kobus K, et al. Cost-effectiveness of HPV16,18 vaccination in Brazil. Vaccine 2007;25(33):6257–70.
17 -Goldie SJ, O’Shea M, Campos NG, et al. Health and economic outcomes of HPV16,18 vaccination in 72GAVI-eligible countries. Vaccine 2008;26(32):4080–93.
18 -Goldie SJ, Diaz M, Constenla D, et al. Mathematical models of cervical cancer prevention in LatinAmerica and the Caribbean. Vaccine 2008;26 (S11):L59–72.
19 -Goldie SJ, Diaz M, Kim SY, et al. Mathematical models of cervical cancer prevention in the Asia Pacific region. Vaccine 2008; 26(S12):M17-29.
20 -Kim JJ, Andres-Beck B, Goldie SJ. The value of including boys in an HPV vaccination programme: a cost-effectiveness analysis in a low-resource setting. British Journal of Cancer 2007;97(9):1322–28.
21 -Kim JJ, Kobus KE, Diaz M, et al. Exploring the cost-effectiveness of HPV vaccination in Vietnam: insights for evidence-based cervical cancer prevention policy. Vaccine 2008;26(32): 4015–24.
22 -Diaz M, Kim JJ, Albero G, et al. Health and economic impact of HPV 16 and 18 vaccination and cervical cancer screening in India. British Journal of Cancer 2008;99(2):230–38.
23 -Kim SY, Goldie SJ. Cost-effectiveness analyses of vaccination programmes: a focused review of modeling approaches. Pharmacoeconomics 2008;26(3):191–215.
24 -Gold MR, Siegel JE, Russell LB, et al, editors. Cost-effectiveness in Health and Medicine. New York: Oxford University Press; 1996.
25 -World Health Organization. Macroeconomics and Health: investing in health for economic development: report of the commission on macroeconomics and health. Geneva: WHO; 2001.
26 -World Health Organization Statistical Information System. CHOICE (Choosing Interventions that are Cost Effective). At <www.who.int/choice/en/>. Accessed 29 January 2008.
27 -Evans DB, Edejer TT, Adam T, et al. Methods to assess the costs and health effects of interventions for improving health in developing countries. BMJ 2005;331(7525):1137–40.
28 -Disease Control Priorities Project (DCPP). At <www.dcp2.org/main/Home.html>. Accessed 28 January 2008.
29 -Goldhaber-Fiebert JD, Stout NK, Ortendahl J, et al. Modeling human papillomavirus and cervical cancer for analyses of screening and vaccination. Population Health Metrics 2007; 5(1):11.
30 -Kim JJ, Kuntz KM, Stout NK, et al. Multiparameter calibration of a natural history model of cervical cancer. American Journal of Epidemiology 2007; 166(2):137–50.
31 -Kim JJ, Goldie SJ. Health and economic implications of HPV vaccination in the United States. New England Journal of Medicine 2008;359(8):821-32.
32 -Kou U. Guidelines for estimating costs of introducing new vaccines into the national immunization system. Geneva: World Health Organization, Department of Vaccines and Biologicals; 2002., 2002.
33 -World Health Organization. Adding a vaccine to a national immunization programme: decision and implementation. WHO/IVB/05.18. 2005. At: <www.who.int/vaccinesdocuments/DocsPDF05/ 777_ screen.pdf>. Accessed 1 August 2008.
34 -Goldhaber-Fiebert JD, Goldie SJ. Estimating the cost of cervical cancer screening in five developing countries. Cost Effectiveness and Resource Allocation 2006;4:13.
35 -International Labour Organization. LABORSTA online database. At: <http://laborsta.ilo.org/>. Accessed 21 September 2008.
36 -Hu D, Bertozzi SM, Gakidou E, et al. The costs, benefits, and cost-effectiveness of interventions to reduce maternal morbidity and mortality in Mexico. PLoS ONE 2007; 2(1):e750.
37 -Max W, Rice DP, Sung HY, et al. Valuing human life: estimating the present value of lifetime earnings, 2000. (October 1, 2004). Center for Tobacco Control Research and Education. Economic Studies and Related Methods. Paper PVLE2000. At: http://repositories.cdlib.org/ctcre/esarm/PVLE2000/ Accessed
18 September 2008.
38 -IAVI/PATH. HPV vaccine adoption in developing countries: cost and financing issues. At: <http://www. iavi. org/viewfile.cfm?fid=47496>. Accessed 29 February 2008.
39 -Constenla D, Ortega-Barria E, Rheingans RD, et al. Economic impact of rotavirus vaccination in Panama. Anales de pediatría (Barcelona) 2008;68(2):128–35.
40 -Drummond MF, Sculpher MJ, Torrance GW, et al, editors. Methods for the Economic Evaluation of Health Care Programs. 3rd ed. New York: Oxford University Press; 2005.
41 -Goldie SJ, Grima D, Kohli M, et al. A comprehensive natural history model of HPV infection and cervical cancer to estimate the clinical impact of a prophylactic HPV-16/18 vaccine. International Journal of Cancer 2003;106(6):896–904.
42- Kim SY, Salomon JA, Goldie SJ. Economic evaluation of hepatitis B vaccination in low-income countries: using cost-effectiveness affordability curves. Bulletin of World Health Organization 2007;85(11):833–42.
43 -World Bank. Regional fact sheet. World Development Indicators 2008: Latin America and the Caribbean. At <http:// siteresources.worldbank.org/DATASTATISTICS/Resources/ lac_wdi.pdf>. Accessed 11 September 2008.
44 -Agosti JM, Goldie SJ. Introducing HPV vaccine in developing countries–key challenges and issues. New England Journal of Medicine 2007;356(19):1908–10.
45 -Haug CJ. Human papillomavirus vaccination – reasons for caution. New England Journal of Medicine 2008;359(8): 861–62.
46- Musgrove P, Fox-Rushby J. Cost-effectiveness analysis for priority setting. Disease Control Priorities in Developing Countries 2006; 271–83.















